Slik bygger du en compliance-workflow for regulerte dokumenter
- for 2 døgn siden
- 7 min lesing

Regulerte bransjer som farmasi, juss og finans lever med en ubehagelig sannhet: ett feil ord i et dokument kan utløse sanksjoner som koster langt mer enn selve feilen. Pharma-selskaper risikerer $14,8M per compliance-brudd, og manuelle, ikke-digitale prosesser øker denne risikoen betraktelig. Denne artikkelen gir deg en konkret, trinnvis veiledning for å bygge en compliance-workflow som faktisk fungerer, fra kartlegging av krav til måling av resultater.
Innholdsfortegnelse
Viktige Funn
Punkt | Detaljer |
Unngå store compliance-risikoer | Robuste arbeidsflyter gir sporbarhet og mindre sjanse for kritiske feil. |
Digitalisering gir effektive prosesser | Automatisering kutter tid og kostnader ved revisjon og dokumenthåndtering. |
Edge cases krever ekstra kontroll | Sørg for filvalidering, OCR og god versjonskontroll ved alle unntak. |
Målbar effekt er mulig | Gode KPI-er dokumenterer reduksjon i avvik og revisjonsinnsats. |
Hva er en compliance-workflow for regulerte dokumenter?
Etter å ha sett på hvorfor feil kan få så store konsekvenser, er det essensielt å forstå hva en compliance-workflow faktisk er. En compliance-workflow er et strukturert system for å håndtere dokumenter fra opprettelse til arkivering, slik at alle trinn er sporbare, godkjente og i tråd med gjeldende regelverk.
Kjernen i standardmodellen er fire faser: kladd, gjennomgang, godkjenning og publisering. Standardmodellen inkluderer elektroniske signaturer, rollebasert ruting, versjonskontroll og revisjonsspor for å møte kravene i 21 CFR Part 11 og EU GMP Annex 11. Disse elementene er ikke valgfrie i regulerte bransjer. De er lovpålagte.
Hvilke bransjer er berørt? Her er de viktigste:
Farmasi og life sciences: 21 CFR Part 11, EU GMP Annex 11, MDR
Finans og forsikring: CRR, Solvens II, MiFID II
Juridisk sektor: GDPR, nasjonal lovgivning, kontraktsrett
Energi og industri: ISO-standarder, HMS-regelverk
Regulatorisk krav | Bransje | Nøkkelkrav |
21 CFR Part 11 | Farmasi | Elektroniske signaturer, revisjonsspor |
EU GMP Annex 11 | Farmasi/biotek | Systemvalidering, tilgangskontroll |
Solvens II | Forsikring | Dokumentasjon av risikovurderinger |
GDPR | Alle bransjer | Sporbarhet, dataminimering |
“Et revisjonsspor er ikke bare god praksis. Det er beviset du trenger når myndighetene banker på døren.”
En solid compliance-workflow for oversettelser er spesielt kritisk når dokumenter krysser språkgrenser. Et audit trail som viser hvem som oversatte hva, når og med hvilken terminologi, er avgjørende for regulatorisk etterlevelse.
Nødvendig forarbeid: Kartlegging av krav og funksjonelle komponenter
Etter å ha forstått hovedkomponentene i en compliance-workflow, må dine spesifikke behov kartlegges før dere lager egne rutiner. Mange virksomheter hopper over dette trinnet og betaler prisen under revisjoner.
Start med å identifisere hvilke nasjonale og internasjonale regelverk som gjelder for din virksomhet. Finanstilsynets e-Reg portal er et godt utgangspunkt for norske finansaktører. For farmasøytiske selskaper gjelder det å kartlegge både EMA-krav og eventuelle lokale krav i hvert marked dere opererer i.
Deretter må dere kartlegge de tekniske og organisatoriske verktøyene dere trenger:
ECM-løsning (Enterprise Content Management) for dokumentlagring og versjonskontroll
ERP-integrasjon for automatiske arbeidsflyter og sporbarhet
Elektronisk signaturløsning som oppfyller gjeldende krav
Terminologidatabaser og godkjente ordlister for konsistent språkbruk
Opplæringsprogram for alle som håndterer regulerte dokumenter
ECM-løsninger koblet med ERP gir automatiske arbeidsflyter som sikrer sporbarhet og minimerer manuell ressursbruk i norske regulerte sektorer. Dette er ikke luksus. Det er infrastruktur.
Roller og ansvar må defineres eksplisitt. Hvem har rett til å opprette dokumenter? Hvem godkjenner? Hvem arkiverer? Uklare ansvarslinjer er en av de vanligste årsakene til compliance-avvik. En god [compliance-guide for oversettelser](https://adverbum.com/no/post/compliance guide for oversettelser slik sikrer du) kan hjelpe dere å strukturere disse rollene også på tvers av språk og markeder.

Proffetips: Lag en RACI-matrise (Responsible, Accountable, Consulted, Informed) for hvert dokumenttype dere håndterer. Dette gjør ansvarsfordelingen synlig og etterprøvbar, noe revisorer setter stor pris på.
For virksomheter som håndterer regulatoriske oversettelser på tvers av markeder, er terminologikartlegging særlig viktig. Et begrep som er godkjent på norsk, må ha en nøyaktig ekvivalent på tysk, engelsk og fransk for at dokumentet skal ha samme juridiske tyngde.
Slik bygger du steg-for-steg en moderne compliance-workflow
Når grunnmuren er på plass, er det på tide å faktisk sette opp og kjøre gjennom arbeidsflyten, trinn for trinn. En standard arbeidsflyt gir opptil 60% raskere dokumentbehandling og opp til 60% lavere ressursbruk ved revisjoner.
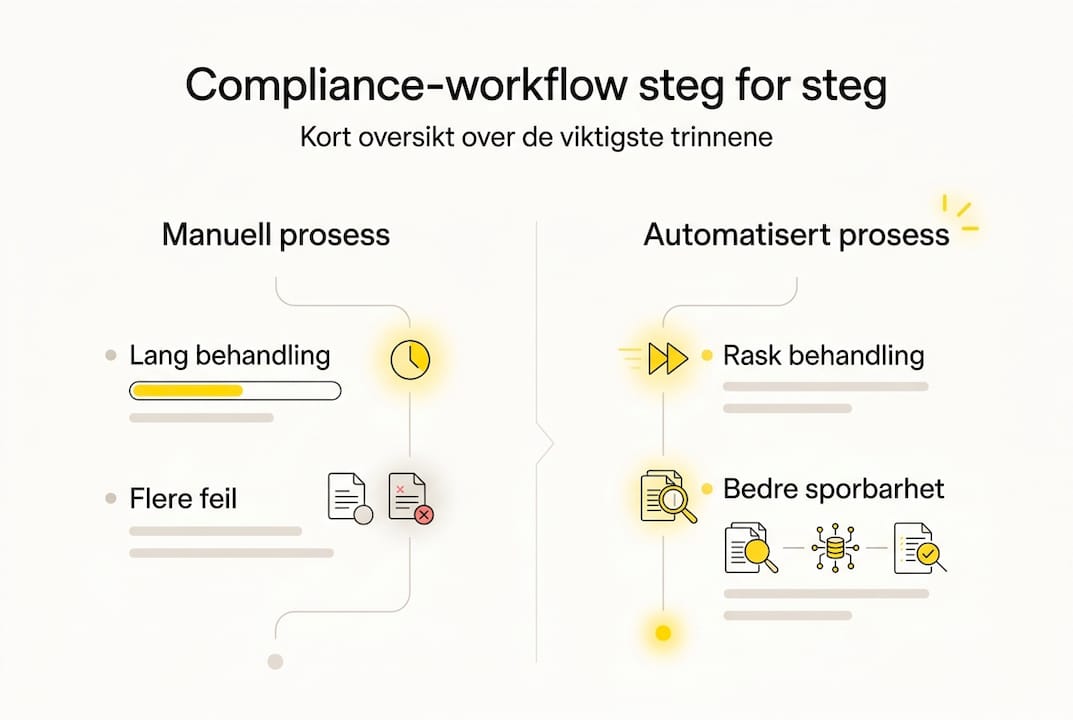
Trinn 1: Klargjør dokumentet og tilpass til regulatoriske krav Identifiser hvilken regulatorisk kategori dokumentet tilhører. Et klinisk studieprotokoll følger andre regler enn en intern HMS-prosedyre. Tilpass malen og metadataene deretter.
Trinn 2: Kladd med kontrollert terminologi Bruk godkjente ordlister og maler fra starten. Feil terminologi i kladdestadiet forplanter seg gjennom hele prosessen og er kostbart å rette opp sent i løpet.
Trinn 3: Rollebasert gjennomgang Rut dokumentet automatisk til riktig fagperson basert på dokumenttype og innhold. En medisinsk tekst skal til en fagrevisor med medisinsk bakgrunn, ikke en generell redaktør.
Trinn 4: Godkjenning med elektronisk signatur Alle godkjenninger skal dokumenteres med tidsstempel og bruker-ID. Dette er kjernen i revisjonssporet og et absolutt krav under 21 CFR Part 11.
Trinn 5: Publisering og distribusjon Kontroller at kun godkjente versjoner distribueres. Gamle versjoner skal arkiveres, ikke slettes, og merkes tydelig som utdaterte.
Trinn 6: Periodisk revisjon og oppdatering Regelverk endres. Sett opp automatiske påminnelser for periodisk gjennomgang av alle aktive dokumenter.
Prosess | Manuell workflow | Automatisert workflow |
Behandlingstid per dokument | 5-10 dager | 1-2 dager |
Feilrate ved revisjon | Høy | Lav |
Ressursbruk ved audit | Svært høy | Opptil 60% lavere |
Sporbarhet | Begrenset | Fullstendig |
Proffetips: Bygg automatisering inn i de trinnene der manuelle prosesser dominerer i dag, særlig ruting og påminnelser. En arbeidsflyt for regulert dokumentoversettelse som er automatisert, reduserer ikke bare feil, men frigjør fagfolk til å fokusere på innholdet fremfor administrasjonen. Se også vår compliance-prosess for oversettelse for detaljer om regulatorisk trygghet i oversettelsesprosjekter.
Vanlige feil, edge cases og hvordan du unngår compliance-feller
Når du har satt prosessen, må du være forberedt på utfordringene. Mange bedrifter sliter med akkurat disse fellene, og de dukker gjerne opp på det verst tenkelige tidspunktet: under en revisjon.
De vanligste feilene er:
Ufullstendige revisjonsspor: Manglende loggføring av hvem som endret hva, og når
Manuell oppdatering av dokumenter: Ansatte som redigerer filer direkte uten å gå gjennom godkjenningsprosessen
Feil håndtering av skannede dokumenter: Skannede PDF-er uten OCR (optisk tegngjenkjenning) er ikke søkbare og ikke sporbare
Manglende versjonskontroll: Flere versjoner av samme dokument i omløp samtidig
Oversett terminologi: Bruk av uoffisielle begreper som ikke samsvarer med godkjente ordlister
Edge-caser som multi-region-innleveringer og bruk av gamle filformater krever formatvalidering og OCR. Versjonskontroll er kritisk i disse situasjonene.
“Den vanligste årsaken til compliance-avvik er ikke ondsinnet atferd. Det er manglende systemer som gjør det enkelt å gjøre ting riktig.”
For virksomheter som opererer i flere land, er multi-region-krav en særlig utfordring. Et dokument som er godkjent i Norge, kan kreve tilleggsvalidering i Tyskland eller Frankrike. Bruk en sjekkliste for regulatorisk oversettelse for å sikre at alle regionale krav er dekket før innsending.
Teknologi og SOPer (Standard Operating Procedures, standardiserte arbeidsprosedyrer) er de to viktigste verktøyene for å motvirke menneskelige feil. Teknologien håndhever reglene automatisk. SOPene sikrer at alle vet hva de skal gjøre når teknologien ikke dekker situasjonen. En gjennomtenkt arbeidsflyt for regulatorisk oversettelse kombinerer begge deler.
Slik vurderer og måler du effekten av compliance-workflowen
Når workflowen er gjennomført, må dere vite om tiltakene faktisk gir ønsket effekt. Dette betyr å måle, analysere og forbedre kontinuerlig.
De viktigste KPI-ene å følge er:
Dokumenthåndteringstid: Hvor lang tid tar det fra kladd til godkjent publisering?
Antall avvik per kvartal: Reduseres antallet compliance-avvik over tid?
Ressursbruk ved audit: Hvor mange timer bruker teamet på å forberede og gjennomføre revisjoner?
Feilrate i oversettelser: Andel dokumenter som returneres for korrigering
Versjonskontrolloverholdelse: Andel dokumenter som følger godkjent versjonsprosess
Automatisert workflow gir opptil 40-60% mindre ressursbruk i audits. Dette er ikke bare en kostnadsbesparelse. Det er tid fagfolkene dine kan bruke på verdiskapende arbeid i stedet for papirarbeid.
KPI | Før automatisering | Etter automatisering |
Tid per dokument | 7 dager | 1,5 dager |
Ressursbruk ved audit | Baseline | Opptil 60% lavere |
Antall avvik | Høy | Signifikant redusert |
Sporbarhet | Delvis | Fullstendig |
Tallene er tydelige: 85% av pharma-virksomheter bruker QMS (Quality Management System, kvalitetsstyringssystem), men 46% av nordiske aktører mangler digitale compliance-løsninger. Det betyr at nesten halvparten av virksomhetene i vår region fortsatt er eksponert for unødvendig risiko.
Sammenstill resultater fra perioden før og etter implementering. Bruk konkrete tall, ikke subjektive vurderinger. Revisorer og ledelse trenger dokumenterte bevis, ikke magefølelse. En compliance-sjekkliste for språktjenester kan hjelpe dere å strukturere denne evalueringen også for oversettelsesdelen av workflowen.
Vil du ha hjelp til sikker compliance og oversettelse?
Å bygge en robust compliance-workflow er krevende arbeid. Når dokumentene i tillegg skal oversettes til flere språk og møte regulatoriske krav i ulike markeder, øker kompleksiteten betraktelig. Det er her profesjonell bistand gjør en reell forskjell.
AD VERBUM har støttet regulerte virksomheter i over 25 år med presise, sikre og compliance-tilpassede oversettelser. Vår AI+HUMAN arbeidsflyt kombinerer proprietær LLM-teknologi med fageksperter innen medisin, juss og finans, og sikrer at terminologi, revisjonsspor og regulatoriske krav er ivaretatt i hvert eneste dokument. All data behandles på ISO 27001-sertifiserte EU-servere, uten eksponering mot offentlige skytjenester. Utforsk vår profesjonelle oversettelse, les om vår arbeidsprosess, eller se spesifikt på vårt tilbud innen life sciences oversettelse. Ta kontakt for en gjennomgang av dine behov.
Ofte stilte spørsmål
Hva betyr revisjonsspor i compliance-workflow?
Revisjonsspor er elektroniske logger som viser alle handlinger på et dokument, og gir full sporbarhet for regulatoriske krav. Revisjonsspor kreves av både 21 CFR Part 11 og EU GMP Annex 11.
Hvordan håndtere skannede filer og ulike filformater i workflows?
Bruk OCR-verktøy for skannede dokumenter og implementer formatvalidering for å sikre kompatibilitet og sporbarhet. Formatvalidering og OCR er essensielt for multi-regional compliance.
Hva er risikoen ved manuelle compliance-prosesser?
Manuelle prosesser gir større risiko for feil, tap av revisjonsspor, ressurskrevende audits og potensielt millionbøter. Pharma-brudd koster $14,8M i snitt per sak, og 46% av nordiske aktører mangler digital compliance.
Er compliance-workflow kun nødvendig for farmasi?
Nei, alle regulerte bransjer inkludert energi, finans og luftfart bør ha slike workflows for å sikre etterlevelse og sporbarhet. ECM-løsninger med ERP gir compliance-innbakte arbeidsflyter på tvers av flere bransjer.
Anbefaling